Il pH è il logaritmo in base 10, cambiato di segno, della concentrazioni degli ioni idrogeno (H+, o più correttamente H3O+) in una soluzione ed esprime il suo grado di acidità.
L’acqua pura, a temperatura ordinaria, presenta un pH pari a 7 in quanto la concentrazione degli ioni idrogeno è pari a quella degli ioni ossidrile (OH-) ed entrambe pari a 10-7. Una piccolissima percentuale di molecole di acqua, infatti, si dissocia secondo la reazione:
[6] H2O = H3O+ + OH-
Allorquando il pH risulta inferiore a 7 (indicando pertanto una predominanza degli ioni idrogeno) allora la soluzione assume carattere acido: solitamente, per quanto riguarda le acque minerali, questo si verifica in quelle circolanti in acquiferi silicei o comunque poveri in carbonati, che invece tendono a conferire un carattere basico alla soluzione.
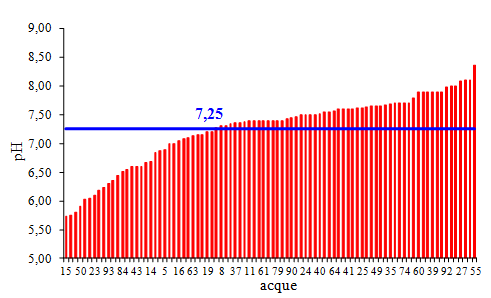
I valori del pH sono indicati in 88 acque (93% del campione) e sono compresi tra 5,73 e 8,37 con una media di 7,25. Nel grafico 8 è riportata una suddivisione delle acque studiate in acide ed alcaline.
Grafico 8 – Classificazione in funzione del pH delle acque studiate
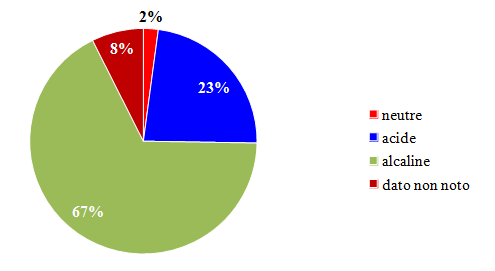
Interessante è il grafico della correlazione tra pH e temperatura delle acque (grafico 9), realizzato considerando ovviamente solo i casi in cui sono indicati entrambi parametri (74 acque su 95, pari al 78%), in cui si osserva una certa (coefficiente R2 = 0,1) ed ovvia correlazione negativa. La migliore interpolazione riscontrata è stata quella di tipo esponenziale e la relativa formula è riportata nel grafico.
Un aumento della temperatura, infatti, favorisce una maggiore dissoluzione di anidride carbonica e di conseguenza una diminuzione del pH, cioè un aumento dell’acidità dell’acqua stessa. Questa regola non viene rispettata da due acque evidenziate dall’ovale rosso.
In queste acque a parità di pH si registra una temperatura più alta del “normale”: questo comportamento è spiegato dal fatto che si tratta di acque mesotermali.
Grafico 9 – Correlazione temperatura/pH
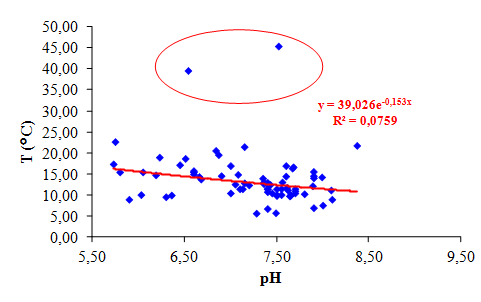
Grafico 10 – pH di tutte le acque studiate (linea blu = media)